Banbrytande DNA-forskning siktar på att lösa cancerns gåta
Kan en krumelur som kallas blobben bli ett avgörande vapen i kampen mot obotlig cancer och andra sjukdomar? I händerna på molekylärbiologen och biokemisten Mats Nilsson kan den bli ett viktigt bidrag. Tillsammans med sitt forskarteam ligger han bakom banbrytande teknik som gjort Stockholm till en internationell hubb för kartläggningen av vårt inre.
Genom hela min forskargärning har jag jobbat för att göra de molekyler som bygger upp livet och våra organ synliga på olika sätt, säger Mats Nilsson.
Kärnan i hans upptäckt är en så kallad hänglåssond, en liten syntetisk DNA-molekyl, som gör det möjligt att få DNA-molekylen fluorescerande i olika färger, vilket gör den synlig digitalt i den vävnad den sitter i. Men för att förstå hur banbrytande det är behöver man först förstå grunderna.
Så fungerar DNA, RNA och proteiner
De flesta organismer som finns på jorden är encelliga. Vi människor har däremot en triljon celler i våra kroppar och kallas därför flercelliga. Cellerna bär alla på en och samma molekyl som heter DNA, det vill säga vår arvsmassa. I DNA-koden finns allt skrivet. Hur cellerna ska byggas upp, hur de ska hamna på rätt plats i kroppen och vad de ska ha för funktion.
– Jag tycker att det är magi. Titta på armarna, säger Mats Nilsson och håller upp dem. De är ju ganska lika varandra eller hur? Hur vet DNA-koden att en cell ska sitta här och inte där.

DNA-koden som en kokbok
I kroppen finns ett tusental celltyper som är helt olika varandra, trots att alla bär på samma DNA. En hudcell är till exempel helt olik en nervcell i hjärnan, eller i ryggraden. Synceller är ljuskänsliga och hörselceller känner vibrationer i vätska. I varje cell finns en uppsättning molekyler, som bär på information om det som styr just den cellens aktiva funktion. Enligt Mats Nilsson är DNA-koden som en kokbok skriven med bara fyra bokstäver, men som allt som allt består av tre miljarder tecken fördelade på 20 000 kapitel. Recepten i kokboken är våra gener.
I varje cell finns hela skriften som talar om hur vi är uppbyggda. Förutsättningarna för vår fantasi, allt vi gör och känner och upplever finns skrivna här. Till skillnad från erfarenheterna vi sedan gör i livet, som skrivs in i en annan kod, i hjärnan, säger Mats Nilsson.
RNA och proteiner
Recepten, som kallas RNA, kan sedan skrivas ut. RNA är en kopia av DNA, men medan DNA sitter i cellkärnan skickas RNA ut ur kärnan och blir då mer åtkomligt. Vi återkommer till det. Men för att det ska bli någon ”action” krävs ännu en beståndsdel, proteinerna.
Proteinerna är det material som bygger upp cellerna och kan också skickas ut ur en cell. Då bygger de kontakt med varandra i ett mellanrum. Cellerna sitter med andra ord i ett proteinnätverk. Proteinerna är den beståndsdel som kan göra saker.
– De är som små maskiner. Vissa bygger upp och andra bryter ner. Båda funktionerna är lika viktiga. De bryter till exempel ner skräp som kommer in i kroppen. Andra proteiner används för att bygga upp. I bland blir det fel som till exempel plack som ger Alzheimer, eller i förhållandevis sällsynta fall, en cancertumör. Allt jobb görs av proteiner.
Blobben - banbrytande wetwear-teknik
Vad är en hänglåssond?
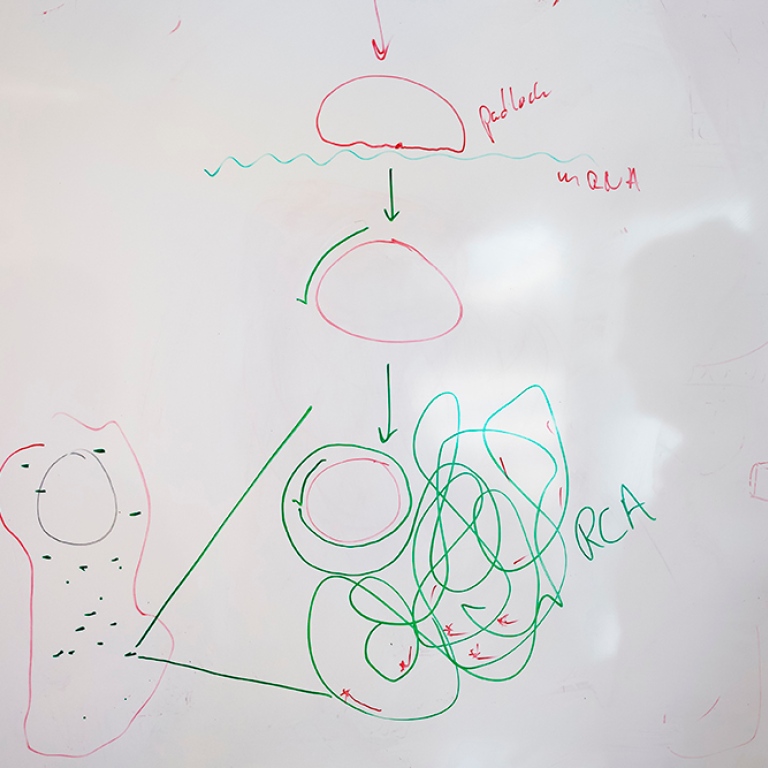
Ett padlock eller en hänglåssond är ett DNA-verktyg i form av en bit syntetisk DNA, som formas till en cirkel med hjälp av ett enzym och är specialdesignad att känna igen en viss målmolekyl. När cirkeln är sluten kan ett annat enzym sedan göra en kopia av cirkeln om och om igen i en ändlös reaktion till en allt längre DNA tråd med hundratals kopior av DNAt som finns i cirkeln. Den långa DNA-tråden bildar tillslut ett nystan, som har förmågan att bli lysande i ett vävnadsprov med hjälp av ett enkelt fluorescencemikroskop. På så sätt kan olika typer av celler bli synliga i ett vävnadsprov. Med hjälp av olika färger kan olika celler också skiljas ut från varandra i vävnaden. Man kan då till exempel tydligt se cancerceller i en tumör.
Det är detta jag har sysslat med i trettio år av ren nyfikenhet, och i förhoppning om att det kan bli användbart. Jag har drivits av tanken: Kan man göra så här? Fungerar detta? Vad skulle man kunna använda det till? Grunden var att jag hoppades att det skulle kunna vara möjligt att synliggöra cancerceller och deras mutationer. Vilket det alltså är.
Under tiden har utvecklingen gått i rekordfart. 1998 var genomet inte helt kartlagt ännu och det fanns inga sekvenseringsmaskiner. Man kände till gener, men inte genernas DNA-sekvenser. Den kemi som fanns tillgänglig för att kartlägga gener var långsam och trögjobbad.
– På den tiden tog det tio år att sekvensera ett genom. Nu tar det kanske ett dygn.
Ett "eureka moment"
Mats uppfinning kallas ”nanoballs” eller ibland bara ”blobbar”. Under en postdok i Holland på ett mikroskopilabb försökte han gå vidare med krumeluren för att se om den fluorescerande (amplifierande) funktionen fungerade.
– Jag tittade i ett mikroskop men såg ingenting. Det visade sig att jag hade stoppat in alldeles för många. När jag spädde ut lösningen såg jag plötsligt mängder av dem ljust lysande.
Det var ett av många ”eureka moments” under karriären. Sammanlagt har de varit omkring fem hittills.
Forskning i kampen mot cancer
Så uppstår cancer
Cancer uppstår på grund av skador i vårt DNA som förändrar ordningen på koden. Den kan förlora en bokstav eller hela sjok med bokstäver, ändra ordningen, eller lägga till bokstäver.
– Det finns många sätt det kan uppstå fel i DNA. Vissa förändringar ger celler möjlighet att dela på sig helt enkelt. Som utbildad biolog har jag Darwins tankar djupt rotade och ser det som en nödvändig konsekvens av det naturliga urvalet, men här inom en individ och inte inom en population av individer.
För kroppen är det däremot inte så bra om celler börjar tappa disciplinen och delar på sig spontant. De tar över och bildar egna ”organ”.
Vi har alla små mutationer som lever i kroppen. De dödar oss inte och man ska faktiskt ha otur om man får cancer. Men sedan är det vissa som sticker iväg och blir elakartade. Nästa eureka moment för mig skulle var om man kan koppla det vi nu känner till till direkt behandling, till exempel: Ta död på alla gröna celler. Att kunna hjälpa människor som är sjuka. Det är nästa steg.
Den snabba tekniska utvecklingen inom life science gör att forskarteamet nu snabbt och med hög precision, med hjälp av sin egen uppfinning, wetwear-tekniken ”nanoballs” eller ”blobben”, kan se skillnad både på vanliga celler och cancerceller, men också på olika typer av cancerceller. Kloner. Nya mutationer. Nya egenskaper.
Kan cancer bli som vilken sjukdom som helst?
– Ja jag tror att man kommer att kunna bota cancer för väldigt många och för andra hålla sjukdomen under kontroll, som med hiv. Men vi har fortfarande inte löst komplexiteten i cancer. Det är så många olika spelare som bygger upp en tumör. Därför är det fortfarande väldigt mycket som återstår. När man kommer med nya behandlingar som funkar, så vet man inte alltid varför det funkar. Det funkar på vissa men inte på andra. Vi försöker förstå varför. Det är den typen av information jag tror att vi kan få med den nya teknik som finns nu.
Är ni framme nu? Eller vad är nästa steg?
Jag skulle vilja göra kartläggningen av DNA-sekvenser på samma sätt som vi redan har sekvenserat RNA. Och inom fler områden. Att få se molekylerna i DNA i själva cellkärnan lysande. Frågan är: Går det att göra samma sak med DNA? Det skulle i så fall vara väldigt användbart för diagnosticeringen och behandlingen av cancer. De flesta mutationer för cancer finns nämligen inte i RNA utan i DNA. Svårigheten här är att DNA är så kompakt.
Och här är vi tillbaka där Mats Nilsson var i början med grundforskningsfrågan. Går det att göra?

Snabb teknikutveckling inom life science
Viktiga tekniska landvinningar
- 2000 - RNA, den kod som DNA skickar ut som ett recept för aktivitet i kroppen har varit möjligt att fastställa/kartlägga under de senaste 25 åren.
- 2008 blev det möjligt att kartlägga DNA/RNA genom effektiva sekvekvenseringsmaskiner
- 2013 publicerade Mats Nilssons forskargrupp metoden "in situ sekvensering", en av de metoder som används inom forskningsmetoden ”Spatial Omics”. *
- 2015 kom tekniken ”Single cell genomic”, en maskin som gjorde det möjligt att mäta RNA i enskilda celler. Det innebar att man kunde börja klassificera olika typer av celler. Tricket var från början att göra provröret mindre och mindre tills det blev lika litet som cellen. Nu finns det en maskin som enkelt gör jobbet. Man stoppar cellerna i en maskin som fördelar dem genom små vätskedroppar i en olja. I varje vätskedroppe finns en cell och en reagens som göra RNA-molekylerna identifierbara. Till varje cell finns också en etikett i form av DNA. Resultatet blev ett stort globalt projekt ”The Human Cell Atlas”.
- 2020 kom möjligheten att placera ut cellerna från single cell-maskinen i vävnaden, med hjälp av en teknik som utvecklats i Mats Nilssons labb, för att på så sätt göra en cellkarta.
*Spatial omics
Spatial omics är ett teknikområde, ett sätt att närma sig en forskningsfråga genom en kombination av metoder. En experimentell vetenskaplig approach skulle man kunna kalla det. 2020 utsåg den vetenskapliga tidskriften Nature Methods Spatial transcriptomics till årets metod.
Mats Nilssons forskargrupp

Forskargruppen som består av tolv forskare från hela världen, bioteknologer, biomedicinare, bioinformatiker och en kirurg, har sitt säte på Scilifelab. Där finns den teknik som behövs för så avancerad forskning. Spetskompetensen och tillgången till högteknologisk utrustning gör att forskargruppen även erbjuder sina tjänster till grupper i hela världen som har en frågeställning och prover, till exempel medicinska kliniker.
Senast uppdaterad: 30 januari 2024
Sidansvarig: Kommunikationsavdelningen

