Forskare avslöjar hemlighet bakom spermiers rörlighet
Forskare vid Stockholms universitet har avslöjat dolda finesser om hur spermier aktiveras från passiva åskådare till dynamiska simmare. Denna förändring är en avgörande pusselbit under resan mot befruktning och den beror på aktiveringen av en unik jontransportör. Studien publicerades i tidsskriften Nature.
Föreställ dig spermier som små äventyrare på sin färd mot den ultimata skatten, ägget. De har ingen karta, men de utnyttjar något ännu mer extraordinärt: kemotaktiska ämnen. Det handlar om kemiska signaler som frigörs av ägget och likt en sirens lockrop attraherar och aktiverar spermierna. När dessa signaler binder till receptorer på spermieytan utlöses en serie händelser, vilket påbörjar rörelsen mot ägget. I detta intrikata scenario är en nyckelspelare ett protein känt som "SLC9C1."
Det finns enbart i spermieceller och är vanligtvis vilande. Men när kemotaktiska ämnen interagerar med spermieytan, förändras allting.
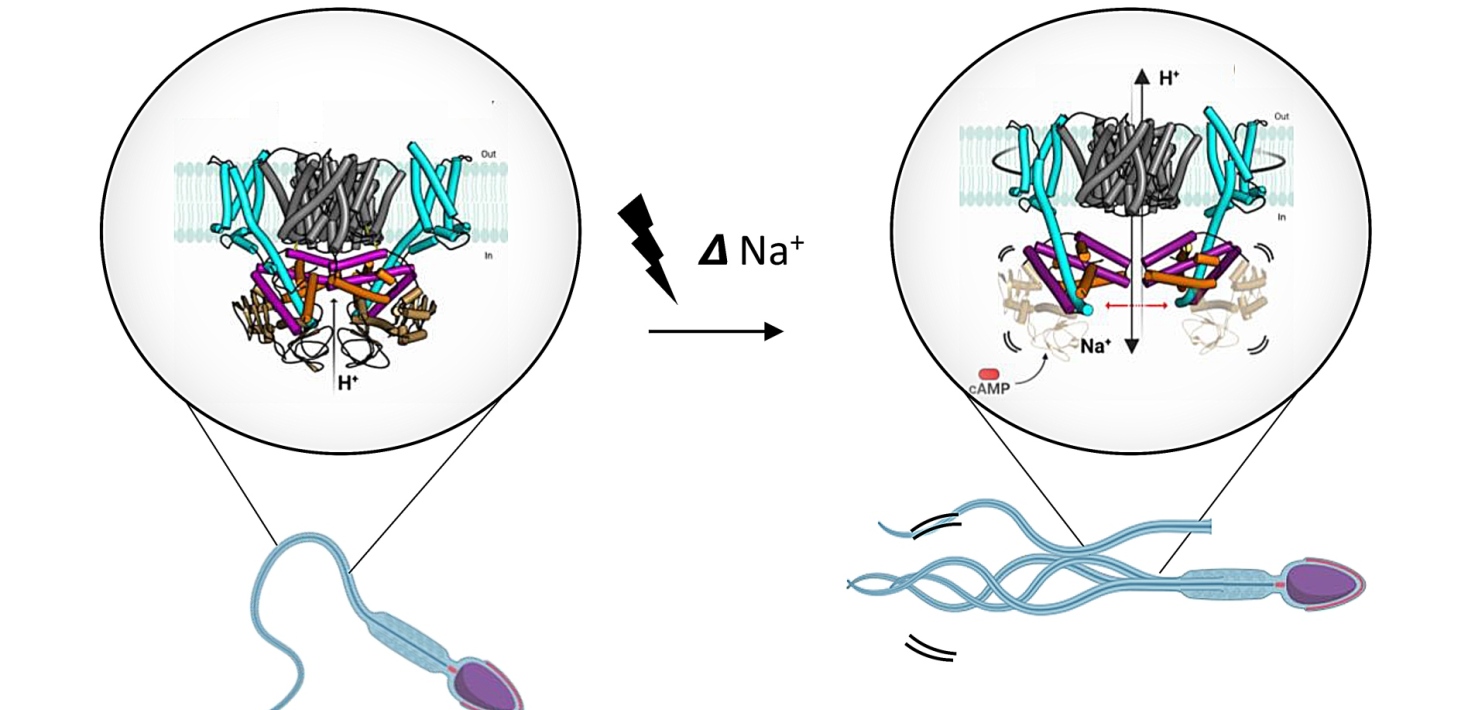
– SLC9C1 fungerar som ett mycket sofistikerat utbytessystem. Det byter ut protoner från insidan av cellen mot natriumjoner från utsidan, vilket tillfälligt skapar en mindre sur miljö inuti spermierna. Denna förändring i den interna miljön skapar förutsättningar för ökad spermierörlighet, säger David Drew, professor i biokemi vid Stockholms universitet.
Aktiveringen av proteinet drivs av en spänningsförändring som uppstår när kemotaktiska ämnen binds. För att åstadkomma detta använder SLC9C1 en unik funktion som kallas en spänningskänslig domän (VSD). Vanligtvis är VSD-domäner förknippade med spänningsstyrda jonkanaler. Men i fallet med SLC9C1 är det något verkligt exceptionellt inom transportörernas område.
Forskare, ledda av David Drew, har avslöjat hemligheterna bakom SLC9C1:s inre funktion.
– Den spänningskänsliga domänen reagerar på spänningsförändringen genom att trycka sin stavlika S4-helix inåt. Det öppnar upp för jonutbyte genom SLC9C1 och driver i slutändan spermiernas rörlighet, säger David Drew.
– Transportörer fungerar mycket olikt jämfört med jonkanaler, och VSD domänen är kopplad till proteinet på ett sätt som vi aldrig sett förut, eller ens kunnat föreställa oss. Det är spännande att se hur naturen har utvecklat detta. Vi kan lära oss från detta och i framtiden kanske skapa syntetiska proteiner, som kan aktiveras genom elektrisk spänning. Det kan också bidra till att utveckla nya preventivmedel för män genom att blockera detta protein, nämner David Drew.
Studien publicerades i tidsskriften Nature. Forskningen gjordes möjlig tack vare finansiering från Europeiska forskningsrådet (ERC) i form av bidraget EXCHANGE.
Senast uppdaterad: 30 oktober 2023
Sidansvarig: Kommunikationsavdelningen

